NMN 治疗可提高大脑相关血管细胞的存活率,并防止糖尿病等代谢疾病中的有害压力。

Published: 3:20 p.m. PST Dec 26, 2020 | Updated: 1:01 p.m. PST Sep 29, 2021
糖尿病病例在全球范围内继续急剧上升。 这些患者更容易中风,出血性中风的风险增加 50%——大脑中的血管破裂。 这被认为是由糖尿病发展过程中脑相关血管细胞(内皮细胞)功能障碍引起的。 尽管科学家们知道这种分解是由有害氧离子(氧化应激)引起的炎症和细胞压力引起的,但如何治疗这种情况仍然难以捉摸。
Luo 及其同事在学术期刊 《FEBS Open Bio》 上发表了一篇论文,提供了补充烟酰胺单核苷酸 (NMN) 可以保护小鼠大脑相关内皮细胞免受氧化应激和功能衰退的证据。 该研究表明,向小鼠内皮细胞补充 NMN 还可以减少细胞死亡并改善细胞的能量工厂——粒线体的功能。 这些发现可以转化为预防糖尿病患者的脑内皮细胞分解和最终的出血性中风。
NMN 改善氧化应激后脑血管细胞的活力
在他们的实验中,研究小组发现 NMN 可以保护在用氧化应激诱导分子过氧化氢处理的实验室培养皿中培养的小鼠内皮细胞。 用过氧化氢处理 12、24 和 48 小时导致细胞存活率逐渐降低。 更重要的是,额外增加NMN补充浓度(300至500 μM)有助于提高细胞增殖率。 这些结果表明,NMN 可以逆转氧化应激对大脑内皮细胞的不利影响,这种不利影响是由糖尿病等代谢紊乱引起的。
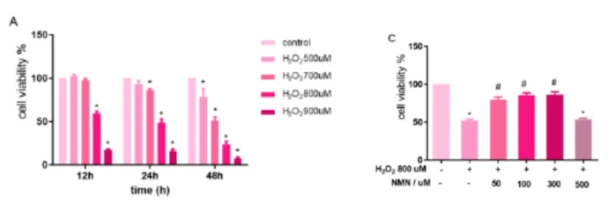
(Deng et al., 2020 | FEBS Open Bio) NMN 治疗可保护脑内皮细胞免受有害的氧化应激。 (A) 显示增加浓度的氧化应激诱导过氧化氢处理 12、24 和 48 小时导致逐渐减少。 (C) 显示用 NMN 处理细胞可挽救高达 300 至 500 μM 浓度的细胞存活。
NMN 增强氧化应激后的粒线体健康
为了确定 NMN 诱导的细胞存活增强是否来自粒线体健康的改善,科学家们检查了粒线体膜的结构完整性。 在有害的过氧化氢处理后,他们发现粒线体膜的渗透性更高,表明结构完整性降低。 在过氧化氢处理中添加 NMN 可恢复粒线体膜电位,表明粒线体已恢复健康。 这些结果表明,NMN通过改善粒线体膜的完整性和健康来增加氧化应激下的细胞存活率。
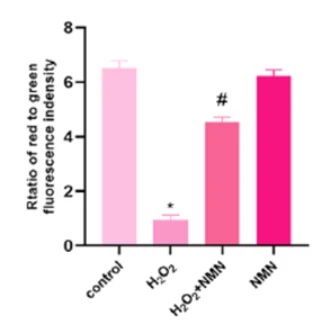
(Deng et al., 2020 | FEBS Open Bio) NMN 可防止氧化应激诱导的线粒体损伤。 红色与绿色荧光的比率表明粒线体膜通透性——离子穿过线粒体膜的能力。 较高的比率代表较低的膜渗透性,表明结构完整性较高。 在这个实验中,NMN 在用过氧化氢(一种引发氧化应激的分子)处理细胞后恢复了粒线体膜的结构完整性。
阐明 NMN 对细胞通路的影响
为了阐明 NMN 如何从氧化应激的毒性作用中拯救细胞,研究人员检查了蛋白质 NF-ĸB 和 NAMPT 的水平,因为它们的水平会随着炎症和疾病而波动。 NF-ĸB 是一种蛋白质复合物,可协调免疫反应以及细胞对氧化应激的反应,而NAMPT是细胞中的一种酶,可从烟酰胺合成NMN。 Luo和同事在过氧化氢处理后发现,NMN增加了NAMPT水平并降低了NF-ĸB水平。 NAMPT 和 NF-ĸB 水平的变化表明 NMN 治疗分别改善了 NAD+ 生物合成和减少炎症。 这种见解可以帮助研究人员了解 NMN 发挥作用的细胞机制,从而为靶向这些细胞途径制定更好的疾病介入方法。
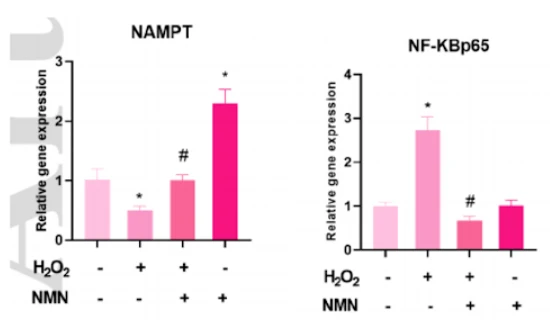
(Deng et al., 2020 | FEBS Open Bio) NMN 对小鼠脑内皮细胞的处理导致氧化应激对 NAMPT 和 NF-KB 的影响逆转 。 左图显示引起氧化应激的过氧化氢处理导致NAMPT水平降低,而NMN逆转了这些影响。 右图表明,过氧化氢处理促进了 NF-KB 水平的显著增加,而添加 NMN 则逆转了这种效果。
“总之,我们的研究结果表明,NMN 能够通过调节酶 NAMPT 和 NF-ĸB p65 信号通路来保护 H2O2 损伤的 bEnd.3 细胞免于凋亡,”作者在他们的学术论文中提到了NMN对脑内皮细胞过氧化氢治疗的影响。
脑血管研究的未来方向
该研究指出了改善脑血管完整性以应对糖尿病等代谢紊乱引起的氧化应激的目标。 如果这些发现转化为人类,NMN 补充剂 可能会改善代谢紊乱患者的脑血管功能。
参考文献
Deng, X., Liang, X., Yang, H., Huang, Z., Huang, X., Liang, C., Kuang, Y., Qin, Y., Lin, F. and Luo, Z. (2020), Nicotinamide mononucleotide (NMN) protects bEnd.3 cells against H2O2‐induced damage via NAMPT and the NF‐κB p65 signalling pathway. FEBS Open Bio. Accepted Author Manuscript. DOI: 10.1002/2211-5463.13067
文章来源
https://www.nmn.com/news/nmn-blood-brain-barrier-cell-response-stress
![]()

