
- Sirt1 长寿基因修复DNA和动脉
- Sirt2 长寿基因可以减少体内脂肪和氧化应激
- Sirt3 长寿基因被认为会影响寿命
- Sirt4 长寿基因可以抑制肿瘤并帮助自噬
- Sirt5 长寿基因帮助减少肝脏中的脂肪酸和氧化应激
- Sirt6 长寿基因调节血糖并降低胰岛素抵抗
- Sirt7 长寿基因使心脏受益
Sirt1 长寿基因修复DNA和动脉
SIRT1是在sirtuins家族7家族中研究得最好的。
科学家认为,随着年龄的增长,NAD +利用率的下降会降低肝脏中的SIRT1,同时会增加DNA损伤。 在动脉中还可以看到SIRT1水平的年龄依赖性下降,表明其参与了心血管系统的衰老。
随着SIRT1长寿基因水平的降低,细胞变得更易于凋亡(一种程序性细胞死亡的形式),研究人员认为,SIRT1长寿基因下降是维持DNA修复,凋亡和衰老之间平衡的一种机制。 (衰老细胞是在正常细胞停止分裂而变得像僵尸一样,既没有生命也没有死亡,但是破坏了正常细胞之间正常健康的信号时发生的。)
功效:减少细胞衰老,体内炎症,心血管、肥胖、胰岛素抵抗、脂肪肝等疾 病发生率;
Sirt2 长寿基因可以减少体内脂肪和氧化应激
SIRT2与调节脂肪(脂肪)组织的发育和功能有关。 肥胖者的脂肪组织中的SIRT2较少,而受卡路里限制的小鼠的白色脂肪组织和肾脏中的SIRT2则更多。 这意味着SIRT2表达与减少体内脂肪有关。
SIRT2的另一个突出作用是,它可以用作细胞衰老标记,因为它在衰老(僵尸)细胞中很显着,但在进入凋亡的细胞(死细胞)中却不显着。 但是,科学家们并不认为SIRT2是导致衰老的因素,而可能是衰老过程中细胞发生变化的影响。
功效:减少神经系统疾 病,增加细胞周期调控,脂肪组织发育和功能,对应心脏、肾脏、肝脏、骨骼肌、血管组织的加强和表达;
Sirt3 长寿基因被认为会影响寿命
SIRT3是目前证据表明可以影响人类寿命的唯一信息。
SIRT3基因的某种多态性(遗传变异)在长寿人群中更为常见。 较少的人存活到老年的可能性较小。
缺乏SIRT3的小鼠的特征在于减少的耗氧量和同时增加的活性氧(ROS,通常称为“自由基”)的产生,以及肌肉中较高的氧化应激。
功效:减少氧化应激反应,心肌肥大,脂肪肝和肥胖发生率,调节线粒体代谢和ATP合成,增加葡萄糖动态平衡和代谢能力,增加身体能 量;
Sirt4 长寿基因可以抑制肿瘤并帮助自噬
SIRT4可以充当癌基因(可以将细胞转化为肿瘤细胞的基因)和抑癌基因,这可能取决于受影响的组织类型和特定的肿瘤环境。
当与葡萄糖代谢抑制剂一起使用时,SIRT4显示出增强的抗肿瘤治疗潜力。 有望进行更多研究,以研究SIRT4与化学疗法药物联合使用对葡萄糖代谢及其对自噬的影响(细胞开始将受损和垃圾部分(缺陷)回收成基本成分,从而使细胞自我重塑的条件) )。
功效:减少脂肪酸氧化,调节线粒体代谢,DNA修 复,胰岛素分泌,对血管、胸腺、睾丸、大脑、心脏有改 善调节作用。
Sirt5 长寿基因帮助减少肝脏中的脂肪酸和氧化应激
SIRT5可以帮助消除促进氧化应激的铵,并减轻肝脏中脂肪酸的积累。
功效:具有尿素循环功能,减少氧化应激和脂肪酸氧化。
Sirt6 长寿基因调节血糖并降低胰岛素抵抗
sirtuins 可以参与哺乳动物衰老调控的第一个证据来自缺乏SIRT6的小鼠。 似乎在沉默调节蛋白中,SIRT6耗竭表现出最严重的表型(可观察到的物理特征),因为它似乎对于达到正常寿命是必不可少的。
此类小鼠出生后三周表现出变性和过早衰老的症状,例如皮下脂肪突然减少,颈椎驼背病(脊柱后背脊柱),结肠炎(炎症性肠病),严重的淋巴细胞减少症(白细胞太少)和骨质减少(稀疏)骨头),这些都将在生命的第四周导致死亡。
功效:具备保护端粒、基 因组稳定性、胆固醇稳态、糖酵解和糖异生的调节;减少心肌肥大、脂肪肝变性、炎症、胰岛素抵抗,增加长寿和葡萄糖动态平衡能力;
Sirt7 长寿基因使心脏受益
已显示SIRT7在心脏中具有有益的功能。 SIRT7缺陷的小鼠会出现心脏肥大(肿大)和炎症性心肌病。 SIRT7似乎可以调节心脏细胞的死亡和损伤,并且已经证明可以通过影响ROS(自由基)的产生来阻止应激诱导的心脏肥大。
功效:保护心脏,调节DNA转录,细胞周期性调节,对外周血细胞、脾脏、血管、性腺系统做平衡与保护;
Sirtuins 长寿基因 仅在存在于所有活细胞中的 辅酶NAD +(烟酰胺腺嘌呤二核苷酸)存在下才能发挥功能。
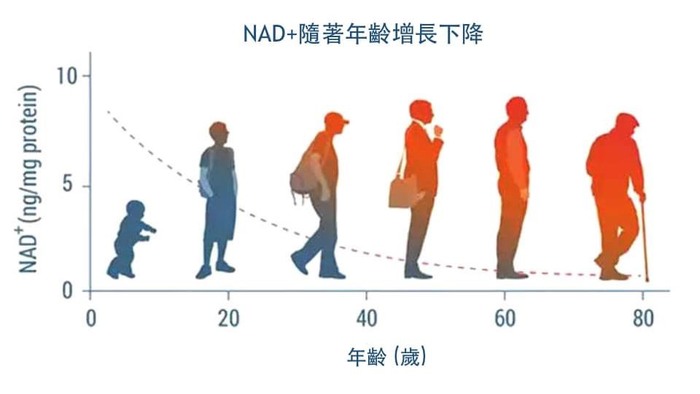
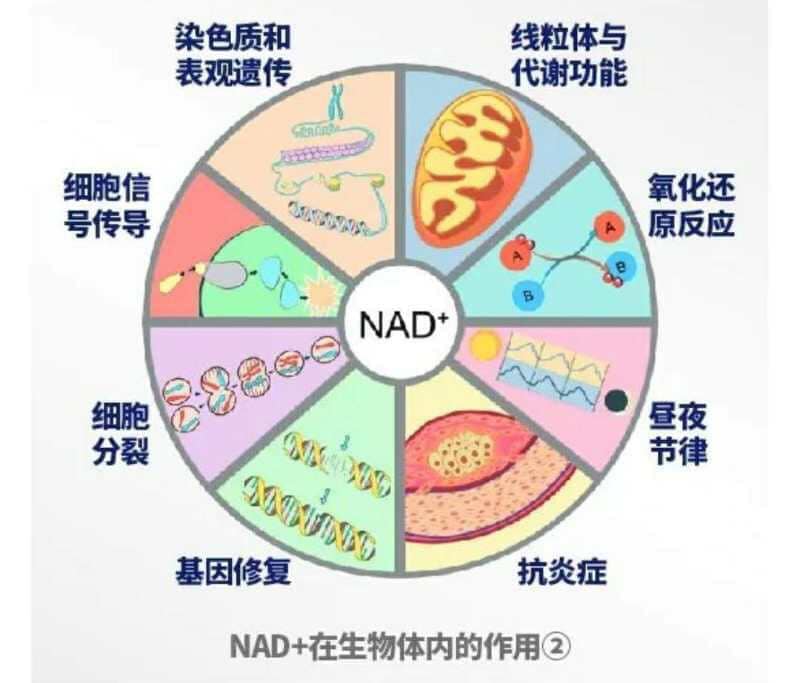
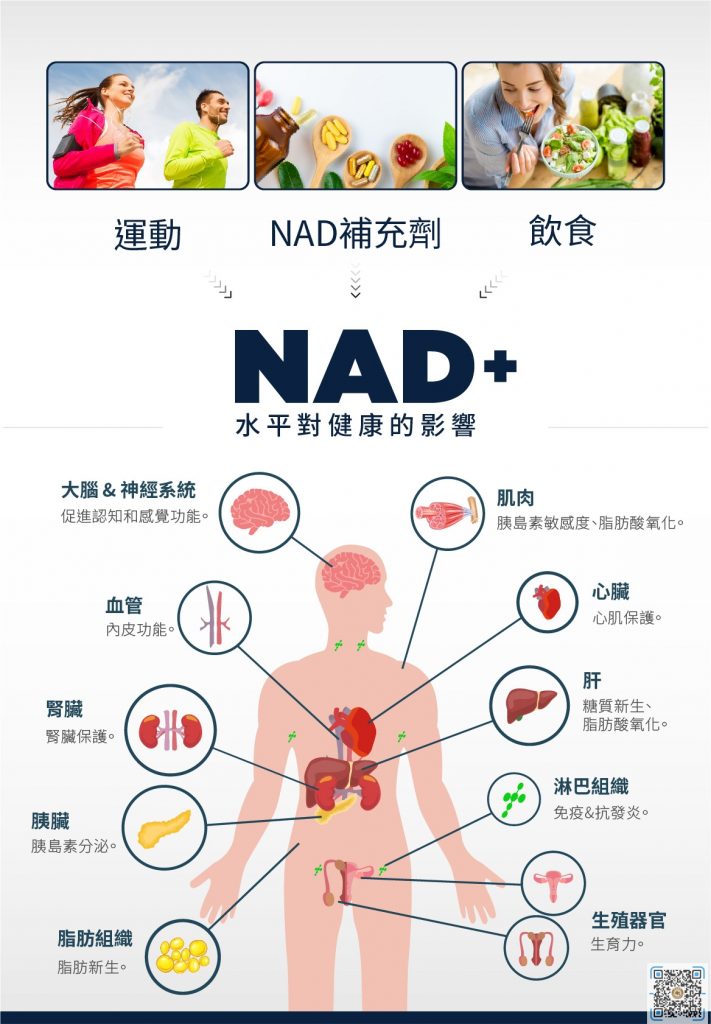
NMN 的抗衰老研究 补充NMN可以快速增加体内NAD+ 的水平,从而激活长寿基因,发挥其应有的作用。
![]()



