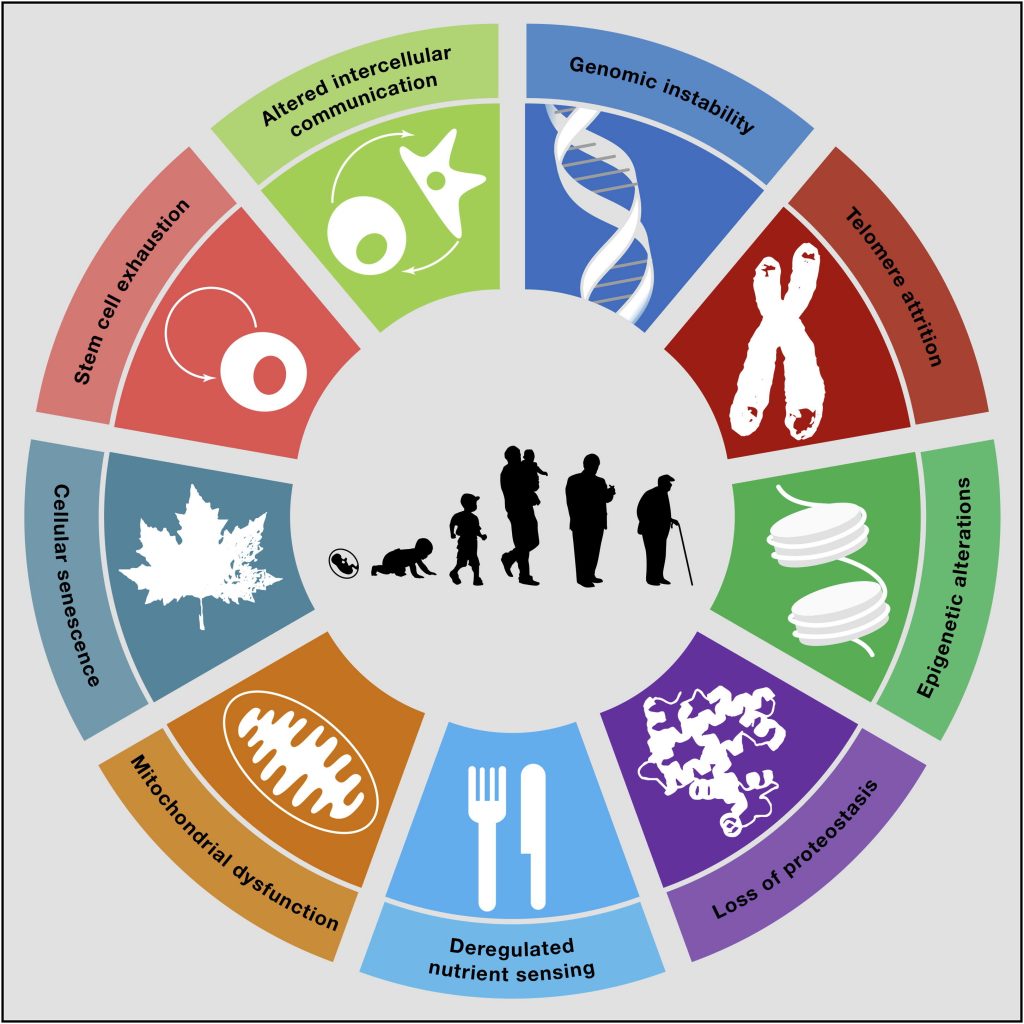
九大衰老指标 — 第一个就是基因的损伤
本文中小编盘点了近些年来和DNA损伤修复相关的亮点研究。
DNA存储着生物体赖以生存和繁衍的遗传信息,维护DNA分子的完整性对细胞发挥正常功能至关重要;外界环境和生物体内部的因素都经常会导致DNA分子的损伤或改变,近年来关于DNA损伤修复相关的研究越来越多,而DNA损伤也和很多疾病的发病直接相关,对DNA损伤修复的新策略或可帮助有效治疗疾病。
本文中小编盘点了近些年来和DNA损伤修复相关的亮点研究。

【1】Nature chemical biology:DNA损伤修复——老问题还有新进展
人体内存在着几万亿个细胞,这些细胞内部一直存在分子的合成,转运和修饰,而在这些过程中难免会发生错误。对于DNA来说断裂的原因有很多种,比如UV照射或染色体受到机械应激。为了保证细胞能够存活并进行适当的复制,机体需要许多机制修复DNA损伤,虽然这个领域的研究已经进行了几十年,但是关于这一基本过程仍有许多未解问题等待科学家们去探究。
近日,来自美国洛克菲勒大学的研究人员在国际学术期刊nature chemical biology上发表了一项最新研究进展,就DNA损伤修复机制进行了进一步研究,揭示了这一过程的一些新信息。
在理想情况下,当DNA链发生断裂,细胞会通过修复机制将其连接到一起继续进行生命活动,但有时损伤修复并不会按理想情况进行,比如染色体的不同区域会融合在一起造成基因重排,进一步导致疾病的发生。为深入了解这一过程,研究人员将研究重点聚焦到一类组蛋白–H2AX上,之前有研究发现这种组蛋白能够参与DNA修复,而研究人员想要对H2AX磷酸化如何介导DNA损伤修复进行进一步研究。
【2】Mol Cell:科学家解析特殊蛋白复合物在DNA损伤修复过程中的作用
我们都知道,人类机体中一种含量丰富名为泛素的蛋白质被认为在回收再利用错误折叠的蛋白质上扮演着重要的角色,但实际上泛素还有另外一个功能,即添加或移除泛素链或可调节新生蛋白质或酶类的活性,实际上该过程称为泛素化作用,其可以通过BRCA1乳腺癌相关蛋白质和抗炎性免疫反应作用来影响DNA的损伤修复。
一种名为BRCC36的特殊酶类可以移除一种对DNA损伤修复和炎性反应非常关键的特殊类型的泛素,但实际上BRCC36并不会自己采取行动,它的作用相当于另外一种名为KIAA0157蛋白所发挥的作用。刊登在国际杂志Molecular Cell上的一篇研究论文中,来自国外的研究人员通过研究报道了多种包含BRCC36的复合物的原子结构,他们发现,BRCC36和KIAA0157都是在结构上相关的蛋白质,但当BRCC36能够移除泛素时(去泛素化,DUB),KIAA0157就并不会结合对移除泛素必要的金属离子,进而并不会完成去泛素化(拟DUB)。

【3】Cell Res:戚益军等小非编码RNA参与DNA损伤修复机制研究获进展
中国科学院北京基因组研究所基因组变异与精准生物医学实验室杨运桂研究组与清华大学生命科学学院戚益军研究组合作研究发现,小非编码RNA(diRNA)及其效应蛋白Ago2调控DNA同源重组修复重要因子Rad51在DNA双链断裂(double strand break, DSB)位点的招募,从而调节DNA修复的作用机制,相关论文在Cell Research在线发表。
DSB是真核生物基因组后果最严重的损伤,可以导致基因突变、基因组不稳定和细胞死亡,因此与包括癌症在内的多种疾病的发生密切相关。真核细胞已演化出了复杂的DSB修复机制,涉及到一系列感应蛋白、传导蛋白和效应蛋白的协调作用。在该合作团队此前的研究中(Cell ,2012),戚益军研究组首次发现了植物细胞中存在一类特异性受DSB诱导并在DSB修复中起到重要作用的小RNA,diRNA (DSB-induced small RNA),随后杨运桂研究组在哺乳动物细胞中确认这类特异性diRNA的存在。diRNA如何介导DSB修复尚不清楚。
【4】Nucleic Acids Res.:DNA损伤修复途径研究中取得新进展
中国科学院生物物理研究所梁栋材院士研究组在最新一期 Nucleic Acids Research 上发表了题为 RecOR complex including RecR N-N dimer and RecO monomer displays a high affinity for ssDNA 的研究成果。
RecFOR是原核生物中重要的DNA损伤修复系统之一。尽管人们对Rec FOR蛋白做了大量的功能和结构研究,然而对于RecFOR同源重组修复机制还知之甚少。在已经报导的晶体结构中,RecR 形成一个donut-like dimer-of-dimers 四体环状结构是RecR结合DNA的功能单位,它参与RecF、RecO与dsDNA 相互结合的模块化作用过程。
在这篇文章中,我们发现来源于Thermus tengcongenesis RecR (TTERecR)在溶液中是以稳定的二体状态存在。通过构建N端和C端的一系列截断体,我们确定了RecR的二体结合面是由N-N端相互作用形成。引起我们兴趣的是,当截去N端16个残基时,RecR16-196在溶液与wild RecR一样是以二体状态存在的,但是它却不能与RecO形成复合物。我们进一步确定了RecR全长和RecR16-196的晶体结构。
【5】Nat Struct Mol Biol:DNA损伤修复因子的结构
神经退行性疾病包括运动失调性毛细血管扩张症(AT,ataxia telangiectasia)和运动失调性毛细血管扩张症样疾病(ATLD),基因组DNA的双链断裂会易化肿瘤或神经退行性疾病形成,是由诸如辐射或环境毒素之类的因素引起。因此,有效修复机制是细胞存活和细胞功能所必需的,所谓的MRN复合物就是修复机制的重要组分,其结构已被阐明。
MRN复合物由核酶Mre11、三磷酸腺苷酶Rad50和蛋白质Nbs1构成,其中Nbs1蛋白负责招募ATM蛋白,ATM蛋白在DNA损伤及损伤部位的早期细胞反应中起重要作用,但还不清楚MRN复合物如何确切地识别双链断裂。为阐明此问题,研究人员对MRN复合物功能缺陷版突变体的结构进行分析,发现数对Mre11分子形成一种由Nbs1蛋白稳定的弹性二聚体,不同的综合征常以某种癌症易感性、辐射或神经退行性病变敏感性为标志,往往与复合物中各亚基的突变与相关,例如:与ATLD相关联的突变存在于Mre11 与 Nbs1连接域内,可能通过减弱彼此的相互作用来抑制ATM激活。
【6】Mol. Cell:中山大学等揭示DNA损伤修复新机制
3月29日,Cell出版社旗下《分子细胞》(Molecular Cell)杂志发表了中山大学肿瘤防治中心和美国德州大学MD安德森癌症中心合作的研究成果,揭示了DNA双链断裂(DSBs)过程中同源重组修复(HRR)的一条重要分子机制。
基因组DNA经常会受到内源或外源因素的影响而导致结构发生变化,产生损伤。在长期的进化过程中,有机体也相应形成了一系列DNA损伤修复机制,以应对损伤的DNA。DNA损伤导致DNA损伤修复途径激活,之后能引起细胞周期节点的激活,从而使细胞有足够的时间去修复被损害的DNA,不能够被正确修复的细胞则会走向凋亡,因此DNA损伤修复途径的激活能够保证细胞基因组染色体的完整性和稳定性。

日本佳丽宝公司日前宣布,该公司研究人员开发出一种促进修复由活性氧导致的DNA(脱氧核糖核酸)损伤的技术,应用该技术,有望研发出更为高效的抗老化护肤产品。
DNA损伤是造成皮肤老化的重要原因,它主要由两个因素导致:一个是紫外线照射,另一个就是活性氧,后者可以使DNA的碱基被氧化。因此促进修复由活性氧导致的DNA损伤对于抵抗皮肤老化具有重要意义。
一般由活性氧导致的DNA损伤可由人体内的碱基切除修复机制自行修复,但需要多种蛋白质协同作业。
近日,刊登在国际著名杂志Nature上的一篇研究报告中,来自布里斯托大学等处的研究者揭示了细胞按优先次序区分存在潜在危险损伤的细胞基因修复的分子机制。文章中,研究者集中研究了单个分子的行为,这就为更好地理解细胞修复途径是如何发生的提供了基础。
形成细胞“说明书”的遗传信息是由DNA分子结构单元来编码的,遗传信息也可以被诸如紫外灯或者烟草烟雾等诱变剂损伤,遗传信息的损伤可以引发细胞死亡或者促使细胞改变其行为,进而引发疾病。
机体细胞可以通过产生能够检测损伤结构单元的蛋白质来进行自我保护,一旦这种特定蛋白质检测到了损伤的结构单元就会将其移除。在大部分细胞中都包含有可以进行快速损伤修复的基因。
【9】PLoS Genet:DNA的损伤修复效率会随着机体老化而下降
随着人类和其它脊椎动物年龄增长,机体中的DNA就会积累突变并且出现重排的现象,最终就会引发一些和年龄相关的机体疾病,包括癌症等;近日,刊登在国际杂志PLoS Genetics上的一篇研究报告中,来自罗彻斯特大学的研究人员通过研究揭示了DNA损伤增加的一种原因,研究者表示,随着机体年龄增加最初的机体修复功能会慢慢下降。
Gorbunova教授说道,长期以来科学家们一直没有一种强大的工具来研究DNA的修复随着年龄增加如何发生改变,如今我们利用小鼠进行研究,就可以测定随着年龄增加,小鼠机体细胞的染色体相同位点DNA修复的效率。当小鼠“年轻”时,其机体细胞DNA链的破碎会通过一种非同源性末端接合(NHEJ)的方式来修复,然而这项研究中,研究人员却发现,随着老鼠年龄增加,NHEJ修复DNA的方式却不再奏效了,而另外一种名为微同源介导的末端连接(MMEJ)的可靠性较低的方式替代了NHEJ;随着MMEJ的修复,DNA链破碎的末端就会通过相似序列的折叠“粘连”在一起,但是该过程会导致DNA片段的缺失及错误的片段粘连到DNA链中。
利用化疗药物cisplatin或oxaliplatin杀伤癌细胞,会造成DNA损伤,因此癌细胞就不能够进行正常的DNA复制。但癌细胞仍然有各种方式进行DNA损伤修复,这直接导致癌症化疗药物不能高效发挥作用,满足病人需求。
近日,来自美国的科学家开发出一种方法,能够在全基因组范围内精确定位DNA损伤修复位点。这一研究进展发表在国际学术期刊Genes & Development。这项新方法或对提高肿瘤治疗效率,解决癌细胞耐药性问题具有重要意义。
文章作者sancer这样说道:“现在我们可以跟同行科学家们说‘只需告诉我们你感兴趣的基因,我们就能告诉你它是如何修复的’,在六十亿个碱基对挑出一个你感兴趣的位点,我们也能告诉你它是如何发生修复的。”

大自然中每一个有机体都会不惜代价保护自身的DNA,但细胞如何精确区分自身DNA的损伤还是入侵病毒外源DNA的损伤依然是个谜底,近日刊登在国际杂志Cell上的一篇研究论文中,来自索尔克研究所的研究人员通过研究揭示了细胞反应系统精确区分上述两种威胁的机制,相关研究或可帮助开发新型的癌症选择性病毒疗法,同样也可以帮助理解为何老化和某些疾病似乎总在为病毒感染敞开着大门。
研究者Clodagh O’Shea教授说道,本文研究阐明了一种基本的机制,即机体如何区分细胞和病毒基因组的DNA断裂来诱发不同的保护宿主的免疫反应,该研究或可帮助解释为何特定的状况,比如老化、癌症化疗以及炎症使我们机体对病毒感染变得更加敏感。
许多因子都会引发DNA断裂,研究者在文章中阐明了名为MRN复合体的一系列蛋白如何检测DNA和病毒的破裂,并且通过组蛋白来放大这种效应;MRN复合体蛋白会开启一种多米诺骨牌效应,激活染色体周围的组蛋白,最终引发一种广泛的效应来帮助机体细胞修复DNA。
来自MIT的研究者们发现,神经元活性可以快速大量激活一些早期反应基因,从而促进大脑的学习和记忆。DNA双链断裂的形成,是一种生理活动,可以快速解除拓扑蛋白对早期反应基因的抑制,从而在神经元中表达这些早期反应基因。这项研究结果,有助于研究人员们研发出新的方法,防治认知下降疾病,例如老年痴呆症。此项研究于近日发表在Cell杂志上。
在此研究之前,研究人员们在小鼠老年痴呆模型上发现,甚至是在疾病的前期,海马区的神经元已经有大量的DNA损伤,即DNA双链断裂。为了研究清楚,这些DNA双链断裂是如何和为什么发生的,哪些基因受其影响,研究人员们使用了神经毒性物质,这些物质可以破坏DNA双链,之后他们提取RNA并进行测序。

近日,一项发表于国际杂志The Journal of Cell Biology上的研究论文中,来自加尼弗尼亚大学的研究人员通过研究发现,一种帮助维持胚胎干细胞(ESCs)身份的特殊蛋白或可促进干细胞的DNA修复,研究者表示,这种名为Sall4的蛋白质在癌细胞中也扮演着类似的角色,其可以帮助修复癌细胞的DNA损伤从而使得癌细胞免于化疗杀伤。
修复破碎的DNA对于ESCs来说非常重要,因为干细胞会将任何突变传递给分化形成的细胞,而小鼠的ESCs就非常善于进行DNA的修复,相比其它分化细胞而言小鼠的ESCs携带的突变会相对较少,但其进行DNA损伤修复的机制目前尚不清楚;于是研究人员就开始检测是否一直ESCs分化的蛋白Sall4在DNA修复过程中扮演着重要的角色。
研究者表示,缺失Sall4的ESCs并不擅长于修复DNA的双链破碎,而双链破碎是DNA损伤的一种灾难性的破坏形式。研究者同时还观察到,当诱导小鼠ESCs发生DNA损伤后,和Sall4相关的蛋白质就会参与进行DNA的修复。
【14】Nat Commun:特殊压力应答器助力DNA修复避免癌症发生
DNA损伤会增加癌症的风险,近日一项刊登在Nature Communications上的研究论文中,来自乔治亚医科大学的科学家通过研究发现,一种当细胞受压力时聚集产生的特殊蛋白活在DNA修复的早期阶段扮演重要角色。在进行DNA损伤修复过程中,一种名为ATF3的活性转录因子3似乎是第一个应答者,其会增加自身的水平,随后寻找并且同另外一种名为Tip60的蛋白结合,最终帮助吸引一大群损伤位点的蛋白质。
研究者Chunhong Yan说,这种蛋白就是所谓的压力应答子,因此当细胞感知到压力,比如DNA损伤时,ATF3就会被诱导激活;ATF3可以同Tip60结合并且促进DNA的损伤修复,就好象其搭档Tip60一样,ATF3直到细胞受到压力时才会低水平表达,而且DNA突变是最常见的一种细胞压力器,随后ATF3就会寻找并结合Tip60来增加不稳定蛋白的稳定性以及表达情况;如果在显微镜下观察DNA,就会发现损伤位点会被ATF3所标记,随后Tip60就会对ATM蛋白进行修饰,来帮助其形成特殊支架以使得其它蛋白可以进行装配。

【15】Science:科学家揭开新型DNA修复解链酶的结构及其相关功能
近日,刊登在国际著名杂志Science上的一篇研究论文中,来自伊利诺伊大学的研究者利用两种创新性的实验技术首次观察到了DNA修复特殊关键蛋白的结构及其相关功能,相关研究或可为解析生物学机制提供新的思路和见解。
两种新型技术的结合,即将同步荧光显微镜同光学捕获技术结合就可以帮助解释对DNA修复关键的蛋白的结构和功能之间的诸多问题;研究者Chemla表示,文章中我们观察了解链酶UvrD的功能-结构的关系,其是在大肠杆菌中发现的一种蛋白质,可以通过将DNA双链进行解开及拉伸来进行DNA链的修复,在人类机体中也存在一种等价蛋白扮演着相同重要的角色,研究者就想去调查到底需要多少UvrD才能够行使好自身的功能,当前科学家们争论的焦点就是到底需要一个UvrD还是两个UvrD的问题。
于是研究者利用染料分子对每一个蛋白进行了荧光标记,这样便于计数,随后在光学捕获技术的帮助下研究者就可以清楚地观察DNA的解链过程,结果发现,单一的UvrD解链酶可以解开DNA但并不会延伸的太远,其会返回到解链起点来回往返,因此研究者将这种状态称之为“受挫状态”,而当利用两个UvrD分子后,其就延伸到很远而且并不会返回起点进行往返过程。
多伦多大学的研究人员发现了严重受损的DNA在单个细胞内的转移和修复过程。
这个发现也许可以揭开癌症机制的各种秘密。多伦多大学的Karim Mekhail教授说科学家以前就已经知道严重受损的DNA会被送至特殊的细胞医院进行修复,然而在此之前人们始终不知道DNA是如何被运送到这些细胞医院。他说他们发现了运送严重受损DNA的细胞救护车和救护车所行驶的道路。
Mekhail通过酵母细胞,发现所谓的DNA救护车实际上是动力蛋白复合物。除此以外,他们还发现修复受损DNA的医院——核孔复合物对受损DNA进行的修复是不正确修复。
这种不正确修复对于DNA来说意义重大,因为DNA蕴含着人体所有的遗传信息,虽然修复后的DNA还能够进行复制,但是给出的细胞建造蓝图已经不正确,这种情况就可能引发癌症。修复受损DNA对于细胞生存的基础条件意义非常重大,因为疾病几乎方方面面都和DNA出问题有关。

近日,来自凯斯西储大学的研究人员通过研究开发了一种新型的可以削弱并杀灭癌细胞的治疗性手段,相关研究发表于国际杂志PNAS上,研究人员表示,他们开发的这种包含遗传和生化的混合型技术可以增加肿瘤抑制性蛋白的水平,从而直接靶向作用癌细胞进而摧毁癌症。
如果实验室的研究发现在动物模型中被证实的话,那么该研究或许就会增强放疗和化疗治疗癌症的效力,而这关键还在于促进“好”蛋白质—p53结合蛋白1(53BP1)的产生,以便可以抑制癌症。研究者Youwei Zhang说道,我们的研究发现或许可以帮助开发新型的基因疗法,来增加53BP1的产量从而杀灭癌细胞,目前我们正在设计增加53BP1水平的分子。
而本文研究还涉及DNA的修复,DNA的损伤是机体DNA化学结构的不规律改变而致,从而会损伤甚至杀灭细胞,而对DNA的致死性改变则是染色体中DNA双链的破碎,DNA双链的破碎往往是通过活性氧而引发。我们的机体可以产生两种修复路径,其中一种可以提供快速但不完整的修复,即将破碎的DNA链连接在一起,而第二种路径则是利用完整未受损伤的DNA链的信息来指导损伤细胞对破碎的DNA进行修复,文章中研究人员就揭开了一种名为UbcH7的基因在调节DAN双链损伤修复过程中的新型作用,剔除UbcH7后可以引发细胞中53BP1蛋白水平的增加。
美国拉斯克基金会近日公布了2015年拉斯克奖(Albert Lasker Award)的获奖者,今年共有3位科学家和一个组织获奖。
今年的拉斯克基础医学奖授予美国布莱根妇女医院的Stephen J. Elledge和美国罗格斯大学的Evelyn M. Witkin。获奖理由是“在DNA损伤反应方面做出的成果,这是一种保护所有活有机体基因组的基本机制”。( 本文转自 生物谷Bioon.com)
![]()