研究人员发现NMN阻碍了一种常见的、难以治疗的乳癌的生长和扩散——转移,并提高了小鼠的癌症生存机率。

Published: 11:10 am PST Jan 31, 2023 | Updated: 4:12 p.m. PST Jan 31, 2023
重大亮点
-
- NMN 能抑制一种常见的乳癌形式-三阴性乳癌(TNBC)–的生长,这种乳癌能逃避典型的治疗。
- NMN 明显改善注射乳癌肿瘤后的小鼠的生存率。
- NMN 通过激活长寿基因 Sirtuin 1来减少乳癌向肺组织的转移,Sirtuin 1能修复DNA并消除细胞压力。
乳癌─一种可怕的诊断─在过去几年中已经超过了肺癌,成为最常见的癌症形式。 更令人不安的是,占15%病例的三阴性乳癌 (TNBC) 逃避了典型的治疗,使化疗成为唯一的选择之一。 这种情况使得人们需要更安全、更有效的方法来治疗 TNBC。
来自中国清华大学的 Luo 及其同事发表在国际学术期刊《肿瘤基因》(Oncogene)上发表论文表明,NMN 限制了小鼠 TNBC 肿瘤的生长。 此外,他们还表明,NMN明显改善了癌症发病后的生存机会,并阻止癌症的转移。 如果这些发现能够转化为人类,它们可能为缓解TNBC的生长和扩散的新方法带来希望。
NMN 减缓肿瘤生长和扩散,同时增加生存机率
为了测试 NMN 如何影响 TNBC 肿瘤,研究人员给免疫缺陷小鼠注射了人类 TNBC 细胞并测量了肿瘤体积,同时给小鼠施用 500 mg/kg/天剂量的 NMN。 在注射肿瘤细胞 48 天后,与未服用 NMN 的肿瘤小鼠相比,NMN 将肿瘤体积减少了 10% 以上。 此外,NMN将肿瘤的生长和在肺部组织中的扩散减少了一半。 这些发现支持NMN显著减缓TNBC肿瘤的生长,并大大限制了肿瘤细胞向其他组织的转移。
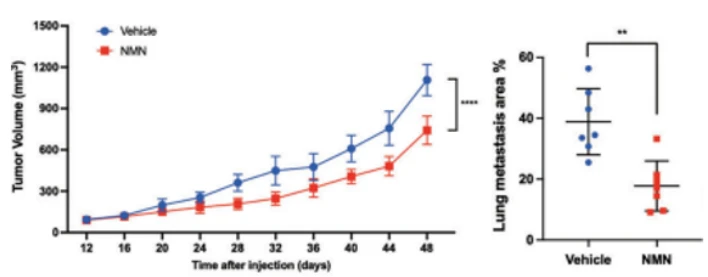
(Jiang et al., 2023 | Oncogene) NMN阻止了10%以上的肿瘤生长,并将其向肺部的扩散减少了一半。 左图:免疫缺陷小鼠被注射了人类乳癌细胞。 48 天后,NMN 介入(红线)产生的肿瘤体积比未经 NMN 介入的肿瘤小鼠(蓝线)小 10% 以上。 右:与未有NMN介入的小鼠(蓝点)相比,用 NMN 介入的小鼠(红点)显示大约一半的肿瘤转移到肺组织。
Luo 及其同事试图找出 NMN 减缓肿瘤生长和扩散的能力如何影响寿命。 他们发现,在注射癌细胞后,NMN将剩余寿命中值延长了约 15%。 这些结果表明,通过阻止癌症扩散,NMN可以延长TNBC发病后的寿命。
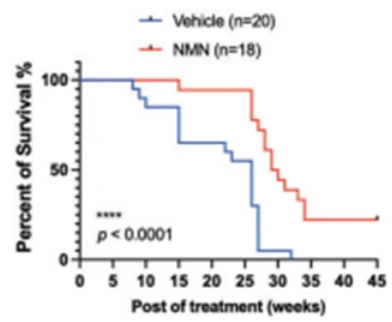
(Jiang et al., 2023 | Oncogene) 用 NMN 介入的肿瘤小鼠的中位寿命延长了约 15%。 NMN 介入的肿瘤小鼠(红线)的中位寿命约为 30 周,而未经介入的肿瘤小鼠(蓝线)的中位寿命约为 26 周——NMN 增加了 15%。
使用 NMN 来增加烟酰胺腺嘌呤二核苷酸 (NAD+) 的水平可激活长寿基因 Sirtuin 1,该蛋白可修复 DNA 并消除细胞中称为活性氧的有害分子。 出于这个原因,中国的研究团队提出 NMN 的抗癌益处源于激活 Sirtuin 1。 沿着这些思路,他们从基因上消除了 Sirtuin 1,发现没有这种蛋白质,NMN 不会显著阻碍 TNBC 转移。 然而,通过保留Sirtuin 1,NMN大大阻碍了TNBC的转移。 这意味着NMN可能通过驱动Sirtuin 1功能来减缓癌症和转移。
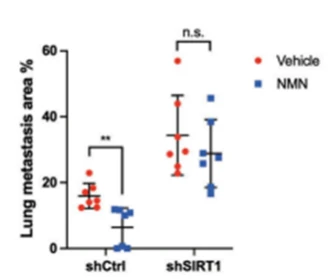
(Jiang et al., 2023 | Oncogene) NMN 减缓癌症向肺部转移的能力取决于 Sirtuin 1 蛋白。 如果不从基因上消除 Sirtuin 1 (shCtrl) 的情况下,经 NMN 介入的癌症小鼠(蓝点)的转移明显少于未介入的癌症小鼠(红点)。 通过基因消除 Sirtuin 1 (shSIRT1) 消除了 NMN 的抗转移作用,表明 NMN 阻止转移的能力取决于 Sirtuin1。
“我们发现 NAD+ 补充剂抑制了 TNBC 的进展,”Luo 及其同事说。
NMN 的抗癌特性可能取决于剂量
有趣的是,Luo 及其同事发现,尽管 NMN 减少了肿瘤的生长,但它并不一定能阻止肿瘤细胞的增殖。 这就提出了一种可能性,即 NMN 增加了抗癌免疫细胞的反应,导致了肿瘤生长的抑制。 更重要的是,在另一项使用较低剂量 250 mg/kg/天的研究中,NMN 对肿瘤生长没有影响。 这意味着 NMN 可能需要像本研究中使用的那样更高的剂量才能发挥其全部抗癌效益。
由于目前通常使用化疗来治疗TNBC,因此NMN可能有助于减缓TNBC肿瘤的生长和扩散,这为抗癌化合物库提供了一个受欢迎的补充剂。 未来的临床研究将有助于确定 NMN 是否可用于治疗人类的 TNBC。
“我们的研究结果提供了针对 NAD+ 代谢的证据,可能是针对 TNBC 的有效介入,希望能将结果转化为人类。 “Luo 及其同事说。
参考文献
Jiang Y, Luo Z, Gong Y, Fu Y, Luo Y. NAD+ supplementation limits triple-negative breast cancer metastasis via SIRT1-P66Shc signaling. Oncogene. 2023 Jan 23. doi: 10.1038/s41388-023-02592-y. Epub ahead of print. PMID: 36690678.
文章来源
![]()

